El tejido óseo es capaz de regenerar rápidamente, debido a las interacciones entre las células que lo conforman: los osteoblastos son los responsables principales de la formación del hueso, mientras que los osteoclastos se ocupan de la resorción del tejido antiguo, en un proceso continuo de remodelado que mantiene los huesos sanos.
Los diferentes tipos de células (osteoblastos, osteoclastos y osteocitos) fueron descubiertos en los años 60 del pasado siglo, y junto con la investigación sobre la matriz extracelular (MEC) y los procesos de crecimiento óseo, se convirtieron en clave para avanzar de forma significativa en técnicas diagnósticas, y más tarde para el desarrollo de productos sintéticos basados en calcio, para su reparación (Bose et al., 2013) como en el caso que hoy nos ocupa:
la bioimpresión de material óseo.

Una forma común de reparar huesos son los injertos óseos. Estos injertos se extraen a menudo de material óseo del propio paciente (autoimplantes), de cadáveres o incluso de algunos animales (aloimplantes). Otros injertos proceden de la reducción de dentina extraída de dientes humanos a polvo, para luego construir implantes.
El problema que tienen los autoimplantes es que solamente son útiles para pequeños daños o fracturas, ya que la extracción de grandes cantidades puede producir fracturas en el hueso de origen, o incluso morbilidad (Bergmann et al. 2010).
Materiales para bioimpresión 3D de huesos
En la actualidad, es común usar materiales que actúan como un andamio, que se descompondrá en el cuerpo siendo reemplazados por el nuevo tejido óseo, aunque en casos complicados se requieren además implantes metálicos. Más recientemente, se ha comenzado a imprimir armazones que imitan las propiedades de la MEC (soporte mecánico, actividad celular y producción de proteína a través de interacciones bioquímicas y mecánicas) para asegurar la adecuación en cuanto en tamaño y forma, para adaptarse de forma exacta a las necesidades específicas de cada paciente.
La limitación de estos armazones deriva de los materiales que pueden ser usados para ser impresos en 3D, pues estos precisan de una cierta resistencia para ofrecer un soporte estructural, además de que deben tener una cierta composición química, y un tamaño y volumen de poros determinado para permitir la formación de hueso en vivo.
Estos materiales varían de un fabricante a otro, aunque todos contienen varios materiales que también se encuentran en el hueso natural; generalmente, están formados por cerámicas con altos niveles de fosfatos de calcio (Komlev et al. 2015, Shao et al. 2016) pero también pueden fabricarse usando biocristal o sulfato de calcio (Zhou et al., 2014, Asadi-Eydivand et al. 2016).
Todos estos materiales son biológicamente activos, y más tarde se disolverán o serán absorbidos en el cuerpo del paciente. Sin embargo, si la férula fuera demasiado gruesa o densa, podría impedir la correcta curación del hueso. A este respecto, el artículo de (Bose et al., 2013) ofrece una revisión de diferentes técnicas de fabricación aditiva para la fabricación de hueso, incluyendo las ventajas e inconvenientes de cada una.
El implante de huesos fabricados en 3D ya ha sido realizado con éxito en animales en China, país que se está revelando pionero en estas tecnologías.
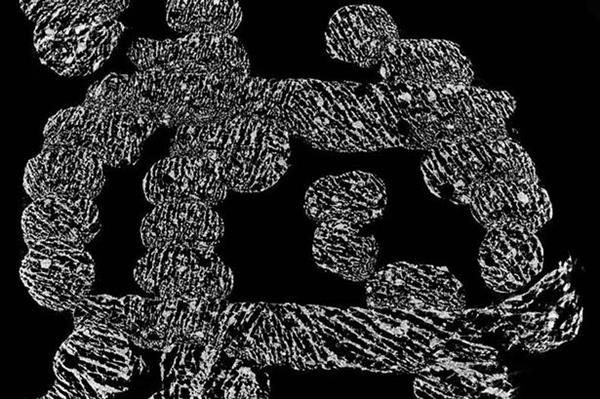
Microtomografía computerizada de un armazón de hueso impreso en 3D. Fuente: 3dprint.
Recientemente, un grupo de investigadores de la Universidad Nottingham Trent están estudiando formas de aumentar la fuerza y durabilidad de estos implantes, y su investigación promete avances que beneficiarían a pacientes con daños severos debido a accidentes, o con pérdida de tejido óseo debido a cáncer u otras enfermedades degenerativas.
Estos investigadores han descubierto que, desarrollando estructuras cristalinas a temperaturas bajo cero dentro del armazón impreso, no sólo se reduce el tiempo de impresión, sino que además los implantes son más fuertes y resistentes al daño.
Estos avances fueron presentados en el Instituto de Física londinense, en una conferencia llamada Printing for the Future, el pasado 19 de enero.
Por otro lado, y como otras impresoras 3D dedicadas de forma específica a trabajar con materiales vivos, se ha creado una máquina especializada en la impresión 3D de huesos.
Esta máquina es obra de la Universidad estatal de Montana State University y Bacterin International. Bacterin es una empresa subsidiaria de Xtant Medical Holdings que se dedica a diseñar y fabricar dispositivos médicos, además de servir de banco de tejidos, por lo que tiene experiencia en implantes y transplantes.
Varios investigadores de Bacterin han colaborado con el Departamento de Ingeniería Mecánica e Industrial de la universidad mencionada, para crear un prototipo de impresora 3D que pueda fabricar implantes de hueso personalizados y readsorbibles para procesos reconstructivos. Todavía no se han revelado más datos de esta impresora, pero puede ser un paso significativo en el campo de los materiales y la bioimpresión.

Hueso fabricado con impresión 3D usando biocristal y fosfato tricálcico (ß-TCP). Fuente: Sciencedirect
Otros artículos de interés:
Fuentes:
Asadi-Eydivand, M.; Solati-Hashjin, M.; Farzad, A.; Abu Osman, N.A. «Effect of technical parameters on porous structure and strength of 3D printed calcium sulfate prototypes», Robotics and Computer-Integrated Manufacturing, Volume 37, February 2016, Pages 57-67
Bergmann, C; Lindner, M.; Zhang, W.; Koczur, K.; Kirsten, A.; Telle, R. Fischer,H. «3D printing of bone substitute implants using calcium phosphate and bioactive glasses», Journal of the European Ceramic Society, Volume 30, Issue 12, September 2010, Pages 2563-2567.
Bose, S.; Vahabzadeh, S.; Bandyopadhyay, A. «Bone tissue engineering using 3D printing,» Materials Today, Volume 16, Issue 12, December 2013, Pages 496-504
Komlev, V.S.; Popov, V. K.; Mironov, A.V.; Fedotov A. Y.; Teterina1, A. Y.; Smirnov, I.V.; Bozo I.Y.: Rybko V.A.; Deev, R.V. «3D printing of octacalcium phosphate bone substitutes». Front. Bioeng. Biotechnol., 08 June 2015.
Shao, H.; He, Y. ; Fu, J. ; He, D. ; Yang,X.; Xie, J. ; Yao, C.; Ye, J. ; Xu, S. ; Gou, Z. «3D printing magnesium-doped wollastonite/β-TCP bioceramics scaffolds with high strength and adjustable degradation», Journal of the European Ceramic Society, Available online.








Deja tu comentario