Con este artículo inauguramos una serie de publicaciones en las que me dedicaré a analizar y exponer con detalle uno de los elementos que más influyen en el desarrollo de la impresión 3D en el campo de la medicina, y sin embargo de los que menos se suele hablar, como es el marco regulatorio y legal que rodea a la implantación de esta tecnología en la práctica médica.
Imagine que su recién nacido, de tan sólo 6 semanas de edad, ha dejado de respirar. En la sala de emergencias del hospital determinan que el diagnóstico es un defecto de nacimiento raro llamado tracheobronchomalacia (TBM), que hace que su tráquea colapse y bloquee el flujo de aire.
Pero entonces el doctor le cuenta que esposible imprimir en 3D una férula que reproduzca la tráquea de su hijo, y la mantenga abierta hasta qué su tráquea se desarrolle, y la férula será reabsorbida por su cuerpo.
A pesar de que esto suena más cercano a la ciencia ficción que la práctica médica actual, los médicos de la Universidad de Michigan ya han hecho esto en múltiples ocasiones.
Esta intervención quirúrgica no sería posible sin la impresión 3D.
Ahora bien,
- ¿qué significa la impresión 3D en términos de regulación médica?
- ¿Cuáles son las ramificaciones legales que influyen en la impresión 3D de dispositivos médicos implantados?
- ¿Puede afectar al uso de elementos impresos en 3D para ensayos quirúrgicos?
Todas estas cuestiones son las que van a acabar determinando la buena implantación y generalización del uso de las tecnologías de impresión 3D en la práctica médica.

Efectivamente, una de las consecuencias menos conocidas del desarrollo de cualquier tecnología innovadora en el campo de la salud y medicina es el desarrollo de marcos regulatorios que garanticen el buen uso y la seguridad de la la misma.
En el caso de la impresión 3D para la fabricación de dispositivos médicos. El Reed Smith LLP Life Sciences Health Industry Group publicó en 2015 un documento técnico sobre esta misma cuestión, 3D Printing of Medical Devices: When a Novel Technology Meets Traditional Legal Principles.
Este documento, imprescindible para entender el marco regulatorio del uso médico de la impresión 3D, abarca cuestiones legales clave cómo el panorama regulatorio, la propiedad intelectual, la responsabilidad civil delictiva, los efectos ambientales, los riesgos para la salud en el lugar de trabajo y los riesgos y la recuperación del seguro médico en EE.UU.
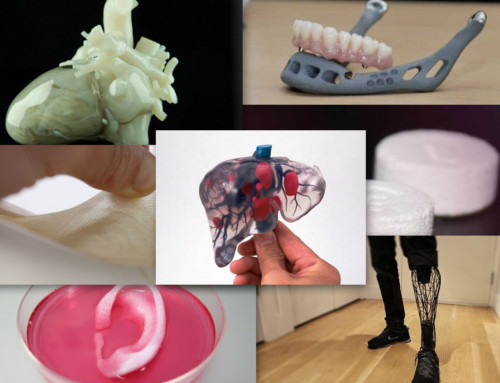
También ofrece una visión general de cómo la tecnología 3D se utiliza actualmente para el tratamiento del paciente, desde la vanguardia de prótesis, a los implantes dentales y faciales, o los modelos de órganos, o férulas traqueales, como el ejemplo citado en la introducción de este artículo.
Retos y riesgos
La impresión 3D forma parte ya de un nuevo capítulo de la revolución industrial. Y, como ha ocurrido tantas otras veces en la historia, la tecnología a menudo se mueve mucho más rápidamente que la ley. Y es por ello que el documento de Reed Smith es tan significativo, porque es el primer intento de analizar de forma integral la impresión 3D en una amplia gama de áreas relevantes para dispositivos médicos.
En este primer artículo sobre el tema del marco legal de la impresión 3D vamos a tomar como ejemplo más avanzado de regulación de la impresión 3D en medicina a la Agencia Federal de Medicamentos (FDA), en Estados Unidos.
Uno de los desafíos legales necesariamente a explorar, durante la implantación o el desarrollo de soluciones de fabricación aditiva en la práctica médica, es el marco regulatorio actual de la FDA para los dispositivos médicos impresos en 3D.
En la actualidad, la FDA considera la impresión 3D como otra forma de fabricación avanzada y, por lo tanto, adapta su marco ya existente a esta tecnología. De hecho, la FDA ya ha eliminado (a través de su procedimiento «510 (k)») aproximadamente 85 dispositivos médicos fabricados a través de la tecnología de impresión 3D.
De la misma manera, la fabricación de dispositivos médicos verdaderamente innovadores a través de la impresión 3D requerirá una aplicación preventiva para su entrada en el mercado (PMA) y, según Steven K. Pollack, director de OSEL, «seguimos a la espera de dispositivos que no era posibles hace unos años, así como de las pruebas que puedan hacerlos posibles, esta es la misión de los PMAs. »

Un campo en eterna exploración
LA FDA en la actualidad está explorando minuciosamente todos los riesgos posibles de responsabilidad civil por daños y perjuicios en la utilización de dispositivos impresos en 3D para uso médico. Sin embargo, desde una perspectiva histórica, la ley de responsabilidad de los productos se desarrolló cuando la fabricación pasó de los artesanos y de los talleres locales a los procesos de líneas de ensamblaje.
La ley de responsabilidad de los productos tendría entonces que volver a adaptarse, ahora que las impresoras 3D tienen el potencial de cambiar el concepto de qué es el producto y quién es el fabricante o el productor.
El marco legal actual será inválido si la producción de los dispositivos médicos deja de formar parte de las empresas ya reguladas en el sector para formar parte de los propios hospitales, de los centros médicos de la universidad, o incluso los despachos de los cirujanos.
Estos nuevos riesgos de responsabilidad van a ser determinantes no sólo para las compañías o las instalaciones que utilizan la impresión 3D para hacer los dispositivos médicos, sino también para los fabricantes de las impresoras. Tener en cuenta estos riesgos desde un principio nos puede ayudar a tratar de evitar potenciales responsabilidades, de la misma forma que también ayudará en la evaluación de las necesidades de cobertura de los seguros médicos.
En este aspecto, el documento de Reed Smith LLP Life Sciences Health Industry Group no sólo señala algunas cuestiones jurídicas desconocidas hasta ahora que pueden resultar de la impresión 3D, sino que también ofrece ideas estratégicas y orientación a los asesores internos sobre mitigación y prevención de riesgos, obligaciones contractuales y cumplimiento normativo.
Como hemos señalado, éste es el primer artículo de una serie que va a tratar sobre los pros y los contras de las diferentes regulaciones existentes en el mundo, tanto en el sentido territorial del término cómo en el sentido cualitativo, y los diferentes procedimientos y riesgos que devienen de dichas regulaciones o de la inexistencia de las mismas, ya que pensamos que la regulación del sector va a marcar mucho el desarrollo y avance de esta tecnología en su aplicación al paciente.
.
Otros artículos de interés:







Deja tu comentario